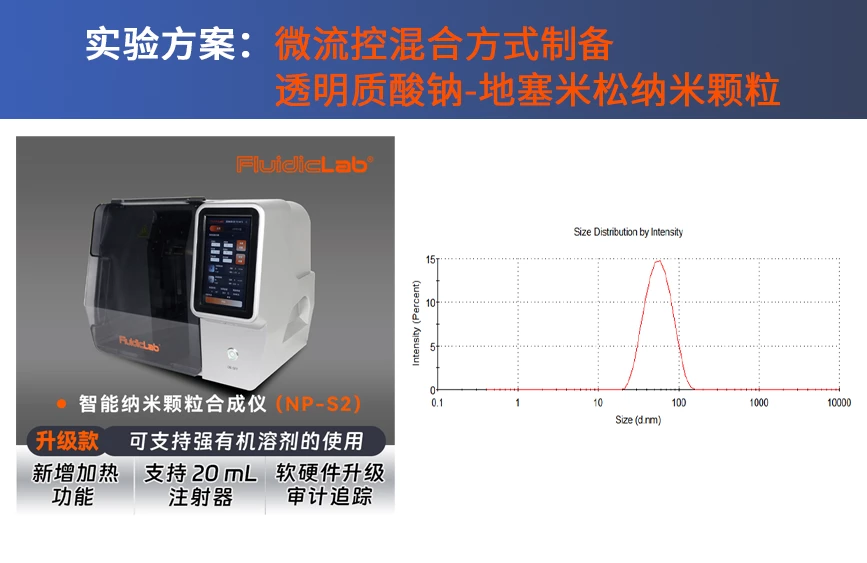
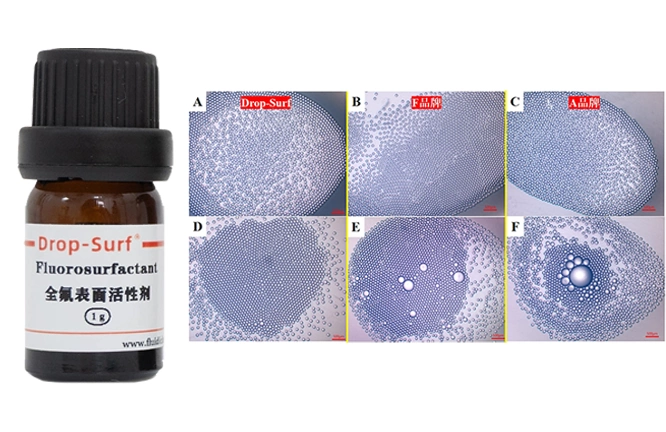
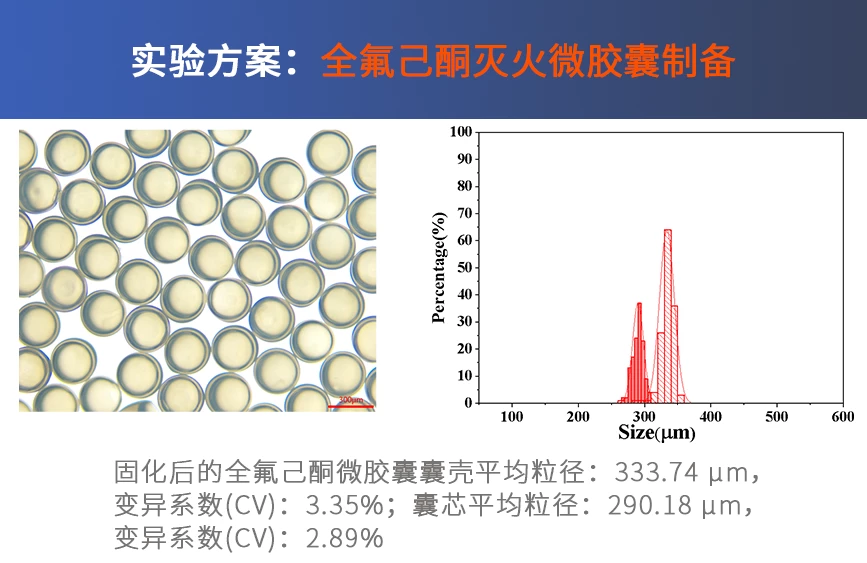
患者来源类器官已成为一种有效的体外癌症研究模型。与2D细胞系、3D细胞系和原代细胞培养相比,患者来源类器官已被应用于药物筛选,以证明基因突变与靶向治疗敏感性之间的相关性。类器官也被用于联合临床试验,以比较类器官的药物反应与相应患者的临床反应。许多研究已经成功地使用类器官来预测癌症患者的治疗反应。利用微流控技术大规模的培养患者来源的类器官,显示了在高通量药物筛选和促进临床治疗决策方面的巨大前景。

四种体外肿瘤细胞培养模型的比较。
二维细胞系:从ATCC中获得细胞后,可在10cm的培养皿中培养。
3D细胞系:从ATCC中获得细胞后,可以在低黏附96孔板中生长。
2D原代细胞:从膀胱癌肿瘤中获得原代细胞后,这些细胞可以在10厘米的培养皿中生长。经过几代后,它们失去了异质性。
类器官:从膀胱癌肿瘤中获得原代细胞后,这些细胞可以在metrigel微滴中生长为类器官。
现有的体外肿瘤模型:
二维细胞系
细胞系来源于获得致癌突变的细胞,他们主要在二维平面上生长。虽然二维细胞系已经在药物筛选上得到广泛的应用。但是,这些模型仍然有很大的局限:
1、无法模拟细胞生长的微环境,无法真实的反映细胞异质性,相邻细胞间、细胞与胞外基质复杂相互作用无法得到真实呈现。
2、虽然许多癌细胞系携带在相应癌症中发现的重要基因突变,但并不一定包含这些癌症所有的基因突变。例如,7种已建立的前列腺癌细胞系均不携带在患者中发现的SPOP突变和FOXA1突变。
3、肿瘤细胞系的基因组成在传代和不同的实验室条件下会发生显著变化。例如,之前对27株MCF7细胞系进行抗癌化合物检测时,发现他们对药物反应非常不同。
3D细胞系
替代2D细胞系的一种方法是将细胞系三维培养形成球状体。与2D培养相比,3D细胞培养明显的改善了细胞形态、力学性能、分化和活力。细胞在3D培养中的药物代谢和分泌行为也使3D细胞团更适合药物筛选。
虽然3D细胞培养克服了2D细胞培养中微环境的问题,但是2D细胞培养中的一些根本问题,如细胞异质性无法呈现、细胞系在传代过程中呈现出的多样性等问题均无法得到解决。
原代细胞培养
原代细胞培养提供了一种更个性化的细胞培养方式。它允许科学家使用与个体患者相同的细胞,而不是使用来源于一个患者样本的细胞来代表患有该特定疾病的所有患者。培养原代细胞包括从新鲜的病人组织中获取细胞并进行体外增殖,但是培养原代细胞仍存在许多困难。
1、许多细胞在培养后不久就停止生长。
2、在多次传代后,分裂速度快慢不同的细胞发生了明显的基因表达分化。
3、多次传代后,细胞种群的比例发生了明显的变化。
患者来源的类器官(PDOs)
PDOs拥有3D细胞系、原代细胞系的优点,又克服了各自的局限,是目前最有前景的细胞培养技术。
简单地说,培养PDOs首先将病人组织粉碎,并将回收的细胞置入基质胶或ECM中,体外培养使PDOs持续生长,最终生长为被称为“类器官”的球体。生长良好的类器官保留了原始肿瘤的遗传图谱和组织学特性。PDOs具有巨大的优势:
1. 肿瘤类器官可以从常规癌症活检获得的组织培养,成功率高,使其可以探索肿瘤发生不同阶段的变化。
2. 基因表达谱在PDOs中往往保持更稳定。
3. PDOs具有高度的可重复性。研究表明在大多数情况下,PDOs表现了对特定药物的同质反应。
4. 肿瘤类器官也可以冷冻保存、扩增、基因分析和迅速进行药物处理。
PDOs用于指导临床治疗
在癌症治疗中,都会在手术切除肿瘤前后都使用药物进行辅助治疗。这些药物主要用于化疗、靶向治疗、放疗,以及近年来的免疫治疗。不同患者有不同的基因背景和体内环境,这可能会影响他们对某些药物的反应。因此,需要一个个性化的模型系统中测试这些药物。
通过研究PDOs和患者对相同药物反应的的相关性,可以检测PDOs在治疗方案选择中的有效性。
临床通过比较胃食管癌患者和来源于患者的类器官对紫杉醇的耐药性,证明了两者之间具有高度的相关性。另一项关于12名患者和患者来源类器官的研究显示,患者对tamoxifen的体内反应与乳腺癌类器官体外反应呈正相关。
2019年的一个临床病例也显示了PDOs在指导肿瘤化疗方案中的有效性。一个结直肠癌转移患者最初接受了联合药物化疗方案,包括药物5-FU、leucovorin和奥沙利铂。不幸的是,化疗完成4个月后肿瘤继续进展。为了决定是否坚持该治疗方案,首先用肝转移活检组织培养出类器官,然后使用药物来处理,并分析了类器官直径和氧化还原比,结果支持继续使用该化疗方案。后续的治疗效果也证明该化疗方案确实减少了肝转移肿瘤的体积。
另外一项临床研究表明,患者和PDOs对放疗的敏感性高度相关,在一个80个病患样本的研究中,68个PDOs显示了和患者相同的反应。
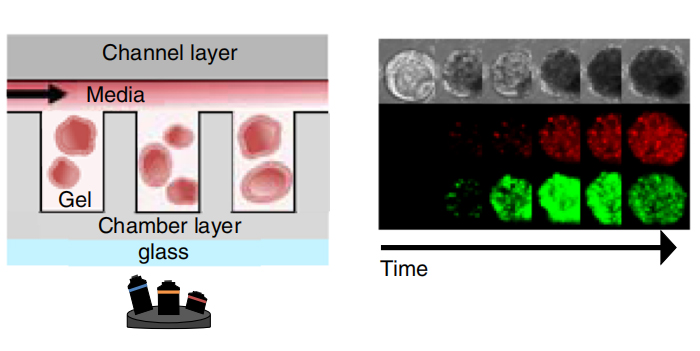
微流控高通量患者来源类器官(PDO)培养方案
本文介绍的方法主要参考以下文献:
* “Automated microfluidic platform for dynamic and combinatorial drug screening of tumor organoids”

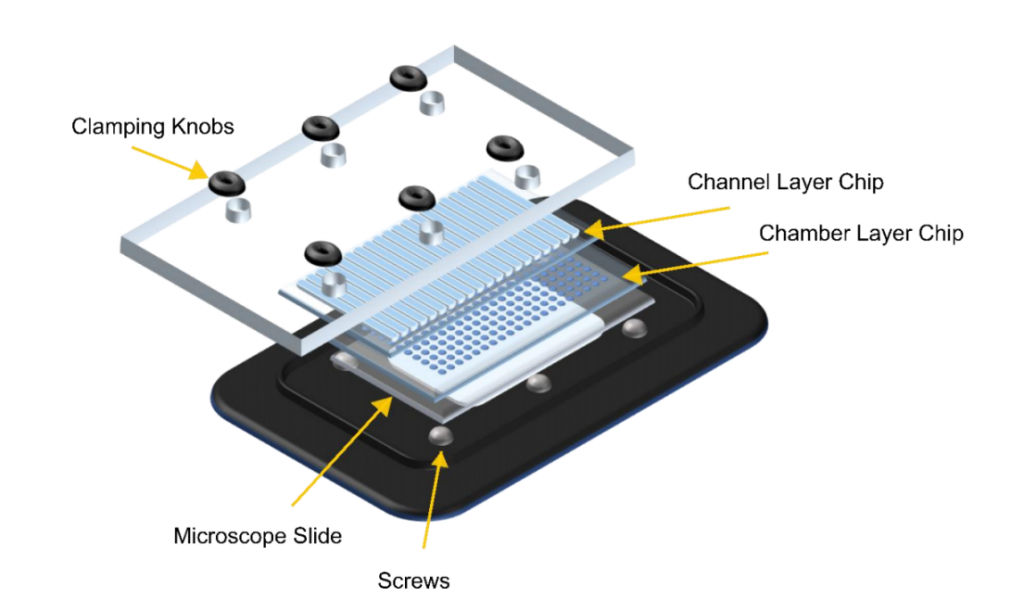

FluidicLab专注提供微流控实验整体解决方案,如有需求,请直接联系我们哦:
021-65103566 / 18616150979(尹先生)